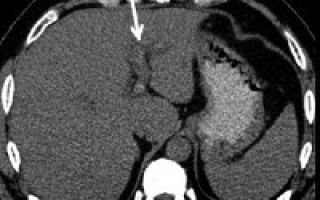
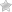Такая система представляет собой дополнительный контур венозного кровообращения, который выполняет функцию очистки плазмы от вредных микроэлементов.
Отдел формируются из больших сосудистых стволов, соединяющихся возле печени. Через брыжеечные вены кровь поступает из кишечника, селезеночная артерия отходит от желудка, поджелудочной. В воротах печени основной сосуд делится на два ответвления, которые транспортируют кровь по левой и правой долям. Доходя до печеночной доли, вены оплетают ее по периферии, потом углубляются внутрь органа.
Размеры воротной вены меняются в результате различных патологий. Длина такого сосуда в норме соответствует 6-8 см, толщина просвета достигает 1,5 см.
Система воротной вены изолирована от других сосудистых бассейнов. Когда возникают проблемы с гемодинамикой в этом отделе кровеносной системы, для нормальной циркуляции активизируются другие сосуды.
Но они не могут проводить через себя необходимый объем крови. Поэтому их работа ограничена.
Организм может компенсировать затруднение кровоснабжения частично при печеночной паренхиме или закупорке воротной вены.
Давление в сосудах нарастает, кровь начинает циркулировать через анастомозы, перетекает полую вену.
Какие сосуды входят
Важнейшие компоненты системы:
- Верхняя брыжеечная;
- Селезеночная;
- Нижняя брыжеечная.
Их характеристики
- Верхняя брыжеечная — выполняет функцию сбора крови из тонкой кишки;
- Селезеночная — собирает кровь от селезенки, желудка и поджелудочной железы.
- Нижняя брыжеечная — несет кровь из ободочной, сигмовидной и прямой кишки.
Воротная вена направляется непосредственно в печень.
На определенном участке она разделяется на две ветви воротной вены – более крупную правую и левую.
Они в свою очередь, разделяются на мелкие венозные сосуды и оплетают печень снаружи и внутри.
Возможные заболевания
К наиболее распространенным болезням относятся:
- портальная гипертензия;
- тромбоз;
- кавернома – она появляется при послеродовом тромбозе;
- пилефлебит.
- Она представляет собой увеличение кровяного давления.
- Портальная гипертензия – это повышение давления крови в портальной системе организма.
- Данная патология в большинстве случаев приводит к образованию тромбов.
- Главными тревожными симптомами, являются:
- диспепсические расстройства;
- необоснованное снижение веса;
- появление признаков желтухи;
- ощущение тяжести в левом боку.
Тромбоз
Это крайне тяжелая болезнь, в результате которой нарушается нормальный отток очищенной крови из-за появления кровяных сгустков в венозном просвете. Это приводит к увеличению кровяного давления.
Основными симптомами тромбоза являются:
- сильные боли в животе;
- тошнота, рвота;
- расстройство стула;
- повышенная температура тела.
В случае перехода хронической формы патологии в прогрессирующую появляется жидкость в брюшной полости.
Вены пищевода становятся крайне расширены, что часто приводит к кровотечениям. Область левого подреберья становится болезненной, селезенка сильно увеличивается в размере.
Пилефлебит
Еще одним серьезным заболеванием является пилефлебит. Это воспалительный процесс, сопровождающийся скоплением гнойного содержимого.
Зачастую его провоцирует острый аппендицит. Данное поражение сосуда является крайне тяжелым состоянием и в ряде случаев заканчивается плачевно.
Симптомы данной патологии очень схожи с проявлениями многих других заболеваний, поэтому диагностируется слишком поздно.
Основные признаки пилефлебита:
- симптомы отравления организма;
- высокая температура;
- боли в животе;
- признаки желтухи;
- возможно внутреннее кровоизлияние в пищевод илижелудок.
По причине врожденного сужения вен происходит кавернозная трансформация, что приводит к образованию каверномы — сосудистого образования, ограниченного сосудистой стенкой и заполненного кровью.
Данная патология чаще всего выявляется у детей и является явным признаком врожденного нарушения формирования систем печени. От чего она появляется – пока не доказано. Однако, уберечь своего ребенка во время беременности может каждая женщина.
У взрослых людей появление каверномы может свидетельствовать о развитии портальной гипертензии на фоне заболевания циррозом или гепатитом.
Перечислим распространенные патологии:
- Портальная гипертензия.
- Пилефлебит.
- Образование тромбов.
- Кавернозная трансформация.
Тромбоз воротной вены – это сложное заболевание, при котором в просвете сосуда появляются сгустки крови, сдерживающие отток после обработки гепатоцитов. Если не лечиться, повышается давление внутри сосуда. Результатом тромбоза является портальная гипертензия.
Причины возникновения болезней:
- цирроз;
- злокачественные опухоли желудочно-кишечного тракта;
- воспаляется пупочная вена, когда вживляются катетеры младенцам.;
- инфекция в пищеварительном тракте;
- травмы внутренних органов;
- плохая свертываемость крови;
- инфекционные процессы.
К редким провоцирующим факторам относится продолжительное употребление оральных контрацептивов.
Признаки портальной гипертензии:
- сильная боль в животе;
- тошнота;
- рвотные позывы;
- диспепсические нарушения;
- высокая температура.
Когда развивается хронический тромбоз, наблюдается частичная проходимость сосудов, возникают такие симптомы:
- В животе скапливается много жидкости.
- Селезенка распухает.
- Просвет кровеносных сосудов пищевода увеличивается.
Тромбоз диагностируется при ультразвуковом обследовании. На мониторе четко отображается плотное образование в венозном просвете. Точные причины заболевания помогают определить компьютерная томография и МРТ.
Кавернозная трансформация
Болезнь развивается на основе врожденных аномалий формирования сосудов. В районе ствола воротной вены появляется кавернома. Это множество маленьких капилляров, компенсирующих проблемы кровоснабжения на данном участке.
Такая трансформация диагностируется у детей, указывает на аномалию формирования сосудов печени. У взрослых пациентов кавернозные образования свидетельствуют о другом расстройстве, развивающемся из-за цирроза или гепатита.
Каверномы появляются в печени в результате действия разных факторов. Новообразование начинает формироваться в капиллярах. Такие проблемы появляются при понижении объемов крови, проходящей через печень. Чаще всего опухоли выявляют возле ствола воротной вены. Такое состояние может развиваться в результате врожденных дефектов формирования системы кровоснабжения, симптомов гепатита или цирроза.
Портальная гипертензия
Расстройство возникает при повышении давления в портальной системе в результате образования тромбов. Нормальный показатель не превышает 10 мм рт. ст.
Перечислим факторы, провоцирующие такое заболевание:
- Цирроз.
- Тромбоз сосудов печени.
- Гепатиты.
- Болезни сердца.
- Проблемы с обменом веществ.
- Закупорка селезеночных сосудов.
Симптомы:
- тяжесть в животе справа под ребрами;
- желтуха;
- ощущение слабости;
- снижение массы тела.
При портальной гипертензии селезенка увеличивается по причине застоя крови в венах. Жидкость в большом объеме скапливается в брюшной полости.
При ультразвуковом сканировании наблюдается увеличение печени и селезенки, доплерография помогает определить размер воротной вены и состояние кровотока. При портальной гипертензии диаметр сосуда увеличивается. Брыжеечная и селезеночная вены тоже расширяются.
Когда и кому обратиться
Лечением подобных болезней занимаются профильные доктора. К таковым относится флеболог. Он расскажет от нормах работы воротной вены и выявит нарушения.
Кроме того, врач может дать направление на проведение исследования другими узкими специалистами – кардиологом, аллергологом, иммунологом и т.д.. Также, в огромном количестве случаев необходима помощь сосудистого хирурга.
Очень важно обращаться в медучреждение при подозрениях на какое-либо нарушение в работе организма.
Пилефлебит
Это один из наиболее сложных воспалительных процессов, протекающих в области воротной вены. Если не лечиться, ткани начинают отмирать, расстройство заканчивается летальным исходом.
Перечислим признаки заболевания:
- симптомы отравления;
- кровоизлияние сосудов желудка, кишечника;
- желтуха;
- озноб.
При обследовании удается определить повышение количества лейкоцитов, интенсивность оседания эритроцитов увеличивается. Такое состояние является признаком гнойного воспаления. Подтвердить диагноз удастся при проведении ультразвуковой диагностики, МРТ, компьютерной томографии.
Диагностика
Перечислим основные способы оценки состояния пациентов:
- Ультразвуковое сканирование.
- Допплерометрия.
- Магнитно-резонансная томография.
- Ангиография.
- Анализ крови.
Все патологии портальной системы определяются с помощью УЗИ. Такой метод обследования отличается точностью, доступностью. Противопоказания к проведению ультразвукового сканирования у пациентов нет. Другие способы диагностики вспомогательные. Допплерометрия позволяет определить скорость кровотока. Ангиография применяется для определения портальных тромбозов.
Анализ крови считается классическим способом выявления патологии сосудов.
Если наблюдается отклонение от нормы, концентрация лейкоцитов и продуктов распада кровяных телец повышается, у специалистов появляется подозрение на развитие болезни.
Если наблюдаются значительные отклонения от нормы, врач проводит дополнительное обследование, выбирает подходящий курс лечения для борьбы с заболеванием.
Основным методом диагностики данной патологии является ультразвуковое исследование.
С использованием допплера можно определить характеристики сосудов и оценить качество кровотока
На экране, специалист обнаруживает небольшое плотное образование, мешающее нормальному кровотоку.
Дополнительными методами выявления тромбоза и сопутствующих заболеваний являются компьютерная и магнитно-резонансная томография.
Заболевания сосудов занимают одно из лидирующих мест по статистике заболеваемости в нашей стране. Огромное количество людей даже не подозревают о наличии у себя серьезных патологий до тех пор, пока не проявятся явные проблемы со здоровьем.
Соблюдение рекомендаций лечащего врача поспособствует улучшению качества жизни пациента и увеличит ее продолжительность.
Воспаления
Сложные патологические состояния возникают из-за действия вирусов. Раздражение тканей сосудов портальной системы отличается повышенной опасностью. Пиелонефрит представляет собой нагноение, которое появляется при острой форме аппендицита. Если оказать помощь пациенту не вовремя, пиелонефрит перерастает в абсцесс.
Воспалительные процессы
Пилефлебит считается одним из самых редких расстройств портальной вены. Симптомы и дополнительная диагностика показывают, что патология может провоцировать тромбы. Пилефлебит появляется из-за нагноения, после которого воспаляется аппендицит. Если своевременно не заняться лечением болезни, пациент умрет.
Поскольку пилефлебит является редким заболеваниям, немного врачей проводят проверку на предмет нагноения в области воротной вены. Диагностика позволяет своевременно определить инфекцию, затем проводится КТ, МРТ, УЗИ, допплерография.
Терапия
Воспаление портальной вены лечится комплексными методами:
- Употребление медикаментов.
- Хирургическое вмешательство.
Медикаментозное лечение подразумевает употребление таких препаратов:
- Антикоагулянты предотвращают появление тромбов, повышают проходимость вен.
- Тромболитики разрезают сгустки крови, очищают просвет сосудов.
- Лекарство назначают только специалисты. Всегда учитываются симптомы заболевания. Если медикаменты не дают желаемого результата, приходится проводить операцию.
Выполняются такие процедуры:
- Тромболизис.
- Ангиопластика.
Главным осложнением после хирургического вмешательства является кровотечение, ишемическое расстройство.
При таких заболеваниях нужно обращаться к квалифицированным врачам.
Главная задача воротной вены печени – отвод крови от желудка, кишечника, селезенки, поджелудочной железы. Воспалительные процессы в области расположения этого сосуда вызывают серьезные проблемы в организме. Полноценная работа печени обеспечивается, благодаря нормальному анатомическому расположению. Это самая крупная железа в организме, ее вес достигает 2 кг в нормальном состоянии.
https://www.youtube.com/watch?v=snWMfccUeIY
Печень очищает тело от токсинов, попадающих в кровеносную систему из ЖКТ. Перерабатывает и удаляет продукты распада эритроцитов. Печень обеспечивает свертываемость крови. Прекращение работы такого органа приводит к летальному исходу.
Источник: https://alfastroy-n.ru/kavernoznaya-transformatsiya-vorotnoy-veny/
Тромбоз воротной вены
Тромбоз воротной вены – это полная или частичная окклюзия ствола воротной вены и ее ветвей тромботическими массами. Патология проявляется абдоминальным синдромом, рвотой, диареей, признаками портальной гипертензии (асцит, спленомегалия, расширение венозных коллатералей), осложняется кровотечением из верхних отделов пищеварительного тракта, инфарктом кишечника и другими состояниями. Основу диагностики составляют методы визуализации – УЗДС, МР- и КТ-ангиография, венография пораженных участков. Лечебная тактика предполагает антикоагулянтную терапию, тромболизис, хирургическую коррекцию.
Тромбоз воротной вены (пилетромбоз) считается достаточно редким явлением, риск возникновения которого не превышает 1% в общей популяции. Его распространенность среди пациентов с циррозом печени варьируется от 0,6 до 26%, что, по-видимому, связано с различием в критериях выборки и диагностических методах.
Заболевание называют причиной 5–10% случаев портальной гипертензии у жителей развитых стран и до 40% – в азиатском регионе (из-за более высокой частоты инфекционной патологии). Распространенность первичного тромбоза у взрослых и детей одинакова.
Гендерных отличий в развитии болезни не выявлено, кроме цирротической обструкции, чаще диагностируемой у мужчин.
Тромбоз воротной вены
Заболевание имеет мультифакторную природу. Тромбоз развивается под влиянием системных и локальных нарушений, участвующих в повреждении сосудистой стенки, усилении коагуляции, замедлении венозного кровотока. Среди наиболее значимых причин отмечают следующие:
- Цирроз печени. Является основным этиологическим фактором, составляя 24–32% случаев тромботической окклюзии. Вероятность тромбоза повышается на поздних стадиях болезни, при необходимости трансплантации органа. Переход цирроза в гепатоцеллюлярную карциному увеличивает частоту внепеченочных пилетромбозов.
- Новообразования. Злокачественные новообразования печеночного или панкреатического происхождения являются причиной 21–24% случаев тромбоза. Развитие патологии опосредовано компрессией или прямой опухолевой инвазией, сопутствующей гиперкоагуляцией, гормональными сдвигами.
- Тромбофилии. Системные нарушения вызваны врожденными дефектами коагуляции – генетическими мутациями (фактора V Лейдена, протромбина, ингибитора активатора плазминогена), дефицитом протеинов C и S, антитромбиновой недостаточностью. К приобретенным факторам относят хроническую миелопролиферативную патологию, антифосфолипидный синдром, пароксизмальную ночную гемоглобинурию.
- Воспалительные заболевания. Патологический процесс может возникать на фоне абдоминальной воспалительной патологии (панкреатита, холецистита, гепатита), инфекционных заболеваний (малярии, брюшного тифа, амебиаза). У детей и новорожденных половина случаев тромбоза приходится на долю омфалита, пупочного сепсиса, аппендицита.
- Травмы и оперативные вмешательства. Воротная вена подвергается повреждению при травмах живота и хирургических вмешательствах на органах брюшной полости (спленэктомии, холецистэктомии, трансплантациии печени). Патология возникает после портосистемного шунтирования, тонкоигольной аспирационной биопсии печени, склеротерапии вен пищевода.
К другим факторам риска тромбоза воротной вены относят беременность, прием пероральных контрацептивов, гиперхолестеринемию. Отмечена роль внутрибрюшной аденопатии, синдрома системного воспалительного ответа.
В детском возрасте окклюзия возникает при врожденных аномалиях сосудистой системы (дефектах межжелудочковой и межпредсердной перегородок, деформации полой вены) и желчевыводящих путей.
Причина 10–30% тромботических стенозов остается невыясненной.
Исходя из современных представлений, пилетромбоз является результатом системных коагулопатий (наследственных, приобретенных) и действия локальных факторов.
Повреждение стенки сосуда опухолью, инвазивными процедурами или травмами характеризуется выработкой цитокинов, активацией тромбоксана A2 и тромбина, усилением адгезии и агрегации тромбоцитов.
Венозный застой при наружной компрессии сопровождается гипоксией эндотелия, накоплением активированных факторов свертывания. Все это запускает формирование пристеночного кровяного сгустка с дальнейшим его увеличением.
Сосудистая окклюзия сопровождается портальной гипертензией, что ведет к изменению системной и внутриорганной гемодинамики.
Печень теряет около 2/3 своего кровоснабжения, но это компенсируется дилатацией печеночной артерии и быстрым развитием сети коллатералей. Вокруг тромбированной вены формируется кавернома, а сама она превращается в фиброзный тяж.
Новообразованные сосуды расположены в пределах желчных протоков и пузыря, поджелудочной железы, антрального отдела желудка, двенадцатиперстной кишки.
Патогенез тромбоза при печеночном циррозе до конца не ясен. Важное значение отводят портальной гипертензии с замедлением кровотока по воротной вене, периферическому лимфангииту, перипортальному фиброзу.
Системное шунтирование крови провоцирует гемосидероз, гепатоциты в зонах гипоперфузии подвергаются апоптозу. В тонком и толстом кишечнике выше уровня окклюзии определяются застойные явления, в желудке – гастропатия.
Брыжеечная ишемия может привести к переходу тромботического процесса на мезентериальные сегменты.
Формальной классификации тромбоза воротной вены не существует. Согласно клиническим рекомендациям по портальной гипертензии, при постановке диагноза учитывают участок тромбоза и его проявления, наличие и характер основного заболевания, степень окклюзии (частичную, полную), вовлеченность внепеченочных сегментов. В зависимости от локализации тромба различают несколько форм патологии:
- Стволовая (трункулярная). Участок окклюзии расположен в стволе воротной вены, дистальнее слияния селезеночной и верхней мезентериальной. Возникает первично или путем распространения из корешкового сегмента.
- Радикулярная (корешковая). Характеризуется поражением корешковых ветвей – селезеночной вены и брыжеечных сосудов.
- Терминальная. Пилетромбоз распространяется на внутрипеченочные разветвления и капилляры, сопровождаясь мелкими или развитыми коллатералями.
Представленная классификация позволяет оценить последствия тромботической обструкции и трудоспособность пациента. При поражении сначала интерстициальных сосудов, а затем крупных стволов констатируют восходящий (первичный) процесс.
Мезентериальный тромбоз, возникающий из-за обструкции воротной или селезеночной вен, называют нисходящим (вторичным). В клинической флебологии также различают острую, подострую и хроническую стадии, последовательно сменяющие друг друга.
Клиническая картина тромбоза воротной вены определяется происхождением, степенью, протяженностью, локализацией, темпами нарастания окклюзии, выраженностью коллатералей.
Частичное тромбирование протекает бессимптомно, выявляясь лишь при инструментальной диагностике, полной обструкции (90–100% просвета) присуще бурное развитие за несколько суток.
Подострая форма прогрессирует на протяжении 4–6 недель, а хронический процесс характеризуется медленным нарастанием симптоматики (от нескольких месяцев до года).
Стволовой тромбоз
Острый стволовой пилетромбоз проявляется резкими болями в правом подреберье и эпигастрии, сочетающимися с метеоризмом, частой рвотой, диареей (нередко с примесью крови).
Быстро нарастают признаки портальной гипертензии – расширение подкожных, пищеводных, геморроидальных вен, асцит. Зачастую выявляют желтуху, недостаточность печеночной функции.
Общее состояние пациентов быстро становится тяжелым, что в основном обусловлено рецидивирующими кровотечениями из желудочно-кишечного тракта.
Радикулярный тромбоз
Радикулярный тромбоз на уровне селезеночного сегмента начинается остро, с боли в левом подреберье, кровавой рвоты и дегтеобразного стула. Увеличение селезенки и субфебрильная лихорадка сочетаются с обычными размерами печени.
В подостром периоде постепенно нарастают спленомегалия, асцит, расширяется венозная сеть на животе.
Терминальная форма патологии выявляется только при распространенном поражении – у таких пациентов обычно определяют увеличенную селезенку, широкие подкожные коллатерали.
Хронический тромбоз
Хронический пилетромбоз не имеет специфических проявлений. Отсутствие аппетита и общая слабость – иногда единственные симптомы болезни. У большинства пациентов выявляют подкожные анастомозы, умеренный асцит.
В 20–40% случаев патология манифестирует кровотечением из варикозных расширений пищевода. Вялотекущие варианты тромбоза воротной вены характеризуются нерезким болевым синдромом, субфебрилитетом, чувствительностью печении при пальпации.
Отмечаются спленомегалия с признаками гиперспленизма, тяжестью в подреберье, исхуданием.
Наиболее опасное следствие острой окклюзии мезентериальных сосудов – инфаркт кишечника с развитием перитонита и полиорганной недостаточности (характерно для 5% случаев). Большинство осложнений длительного пилетромбоза обусловлено портальной гипертензией.
Расширение пищеводных вен у многих пациентов сопровождается кровотечением, риск которого в 100 раз выше при циррозе печени. Выраженное портосистемное шунтирование приводит к печеночной энцефалопатии, вторичным изменениям в желчевыводящих путях (портальной билиопатии, холангиопатии).
При сохраняющихся факторах риска тромбозы могут рецидивировать, осложняться эмболизацией.
Отсутствие специфических признаков тромбоза, необходимость определения предпосылок, уровня, степени и последствий поражения создают потребность в комплексном обследовании пациента. Основой диагностической программы выступают методы инструментальной визуализации:
- УЗАС воротной вены. Обладая высокой специфичностью (60–100%), признано методом выбора при первичной диагностике. УЗДС определяет неоднородный очаг повышенной эхогенности с нечеткими контурами, частично или полностью перекрывающий сосудистый просвет. Допплеровское картирование дает возможность выявить отсутствие кровотока в вене и ее притоках, наличие портосистемных шунтов, каверноматозную трансформацию.
- КТ и МР-ангиография сосудов. КТ с контрастированием дает точную информацию о состоянии венозных стенок, протяженности тромбированных участков, наличии перивисцеральных коллатералей, варикозных вен в забрюшинном пространстве. Магнитно-резонансную ангиографию используют для выяснения состоятельности портального кровотока, оценки просвета шунтов – ее результаты более надежны, чем УЗДС.
- Портальная венография. Используется в случаях, когда неинвазивными методами подтвердить или исключить тромботическое поражение не удается. Контрастная венография выявляет не только стенозы, но и дефекты наполнения от сдавления извне. Однако при установленной проходимости сосуда в ней нет необходимости.
Проводя диагностику пилетромбоза, врачи-флебологи обращают внимание на показатели коагулограммы (увеличение фибриногена, протромбинового индекса, замедление времени свертывания крови), низкий уровень антитромбина.
Выявить варикозно-расширенные вены пищевода позволяет ФГДС, исключить цирроз удается благодаря эластографии и биопсии печени.
Дифференциальная диагностика осуществляется с печеночным шистосомозом, тромбозом нижней полой вены, сдавливающим перикардитом, рестриктивной кардиомиопатией.
Задачами лечебной коррекции являются восстановление проходимости сосуда, предотвращение прогрессирования патологии, устранение осложнений венозной гипертензии. Исходя из остроты процесса, возраста пациента, этиологических и прочих факторов, применяют комбинацию консервативных и радикальных методов:
- Антикоагулянтная терапия. Является лучшим способом для реканализации венозного просвета, но единого мнения о ее применении нет. Длительность лечения антикоагулянтами (низкомолекулярными гепаринами, пероральными средствами) у лиц с острым пилетромбозом составляет от 3 до 6 месяцев, а при хроническом решается в индивидуальном порядке.
- Введение тромболитиков. Регионарный тромболизис (введение стрептокиназы, альтеплазы, тенектеплазы) транспеченочным или трансъюгулярным доступом позволяет обеспечить реканализацию, избежав побочных эффектов антикоагулянтной терапии. При острой тотальной или субтотальной окклюзии может выполняться системный тромболизис.
- Хирургические методы. При неэффективности консервативных мероприятий операцией выбора является дистальное спленоренальное шунтирование. В условиях нарушенной проходимости селезеночного участка накладывают мезентерикопортальный или мезентерикокавальный анастомоз с применением сосудистых протезов.
Варикозные расширения пищевода лечат с помощью лигирования, эндоскопической склеротерапии. В ургентных ситуациях при кровотечении могут производить операции азигопортального разобщения (гастротомию с прошиванием нижней трети пищевода, деваскуляризацию желудка). Тяжелый гиперспленизм требует спленэктомии.
В целом прогноз при заболевании относительно благоприятный. Сгустки могут подвергаться асептическому аутолизу, организации, васкуляризации. Десятилетняя выживаемость для взрослых достигает 60%, а общий уровень смертности составляет менее 10%.
При наличии цирроза и злокачественных новообразований прогноз ухудшается. Иногда тромбы превращаются в эмболы, становятся источником сепсиса. Но своевременное и интенсивное лечение приводит к реканализации сосуда, что сопровождается полным клиническим выздоровлением.
Профилактика рецидивов проводится путем назначения антикоагулянтов.
Источник: https://www.KrasotaiMedicina.ru/diseases/zabolevanija_phlebology/portal-vein-thrombosis
Узи системы воротной вены
Ультразвуковая анатомия
Воротная вена образуется из слияния верхней брыжеечной вены и селезеночной вены. Последняя отходит от ворот селезенки и идет вдоль заднего края поджелудочной железы, сопровождая одноименную артерию.
Картина внутрипеченочного ветвления и печеночных вен определяется сегментарным строением печени. Анатомическая диаграмма показывает вид печени спереди.
MP-ангиография в корональной плоскости является альтернативной методикой визуализации системы воротной вены.
Методика исследования
Внепеченочные сегменты визуализируются на расширенном межреберном изображении. Если данная методика оказывается безуспешной вследствие наложения газа в толстой кишке или неприемлемого допплеровского угла, внепеченочные ветви воротной вены можно сканировать из правого переднего межреберного доступа с поднятой правой рукой, что позволяет увеличить межреберные промежутки.
Зачастую основной перипортальный ствол визуализируется лишь в этой плоскости вследствие того, что акустическое окно, обусловленное печенью, является наилучшим. Ход внутрипеченочных ветвей таков, что лучше всего они визуализируются на подреберном косом скане.
После проведения сканирования в В- и цветовом режимах для количественной оценки перипортального кровотока в воротной вене записываются допплеровские спектры.
Нормальная картина
Ультразвуковая допплерография воротной вены показывает постоянный приток крови к печени, дающий однофазный допплеровский спектр в виде полосы. Изменяя положение тела и режим дыхания, можно управлять кровотоком. Скорость кровотока в воротной вене, например, значительно уменьшается в сидячем положении и на полном вдохе.
- Ультразвуковая допплерография в диагностике патологических изменений воротной вены при различных заболеваниях
- Портальная гипертензия
- Цветовой режим при портальной гипертензии демонстрирует снижение кровотока или даже значительные изменении, такие, как кропоток от печени по воротной вене или селезеночной вене и помогает визуализировать коллатерали.
Тромбоз воротной вены приводит к увеличению сопротивления в системе циркуляции воротной вены. Он может быть результатом цирроза, опухолевой инвазии, повышения свертываемости крови или воспаления.
Кровоток в основной печеночной артерии усиливается, чтобы компенсировать дефицит кислорода, вызванный нарушением перфузии по воротной вене.
По ходу затромбированной воротной вены может отмечаться кавернозная трансформация, приводящая к возникновению гепатопетального кровотока.
Косвенные признаки портальной гипертензии по ультразвуковой допплерографии
- Уменьшение скорости кровотока менее 10 см/с
- Тромбоз
- Кавернозная трансформация воротной вены
Прямые признаки портальной гипертензии по ультразвуковой допплерографии
- Портокавальные анастомозы
- Кровоток от печени
Чрезъяремный внутрипеченочный портосистемный шунт
Установка чрезъяремного внутрипеченочного портосистемного шунта стала первичным методом декомпрессии системыворотной вены. Катетер вводится через внутреннюю яремную вену в правую печеночную вену и затем через ткань печени — в перипортальный сегмент воротной вены.
Это сообщение держится в открытом состоянии благодаря металлическому стенту. Одним из результатов этой процедуры является компенсаторное усиление кровотока в общей печеночной артерии.
Рецидивный стеноз стента или окклюзия его являются частыми осложнениями и требуют повторного вмешательства.
Ультразвуковая допплерография, особенно в энергетическом режиме, играет важную роль в контроле после осуществления интервенционной процедуры.
Внутрипеченочные опухоли
Ультразвуковая допплерография помогает в дифференциальной диагностике неопределенных сосудистых и солидных образований печени.
Аденомы, очаговая узловая гиперплазия и гемангиомы можно отличить от злокачественных опухолей по характерным признакам. Отсутствие кровотока в гиперэхогенном гомогенном образовании позволяет заподозрить гемангиому.
Этот диагноз можно уточнить, определив дополнительные характеристики кровотока при использовании контрастных веществ.
Применение контрастных веществ
В последние годы использование допплеровского и энергетического допплеровского режимов улучшило дифференциальную диагностику внутрипеченочных образований по сравнению с традиционным В-режимом, однако даже у опытных специалистов до сих пор могут возникать проблемы.
Во-первых, некоторые глубоко расположенные образования печени, а также образования у очень полных людей можно визуализировать лишь с неприемлемым допплеровским углом, что ограничивает точность исследования.
Во-вторых, очень медленный кровоток, который часто наблюдается, особенно при небольших опухолях, дает неадекватные частотные сдвиги.
В-третьих, в некоторых участках печени очень сложно избежать артефактов от движения вследствие передачи сердечных сокращений на паренхиму печени.
Ультразвуковые контрастные вещества в сочетании с модифицированной методикой сканирования позволяют помочь в решении данных проблем. Они значительно усиливают внутрисосудистый сигнал, улучшая выявление даже медленного кровотока в мелких опухолевых сосудах.
При болюсном введении контрастных препаратов в картине усиления выделяют несколько фаз. Они могут в какой-то степени варьировать в зависимости от индивидуальных особенностей кровообращения у пациента.
Фазы усиления после внутривенного введения контрастного препарата
- Ранняя артериальная: 15-25 с после введения
- Артериальная: 20-30 с после введения
- Воротная: 40-100 с после введени
- Поздняя венозная: 110-180 с после введения
Доброкачественные образования печени: очаговая узловая гиперплазия и аденома
Доброкачественные образования печени, в отличие от злокачественных, не содержат патологических шунтов. В результате они остаются усиленными даже в позднюю венозную фазу. Это характерно для очаговой узловой гиперплазии и гемангиомы.
Очаговая узловая гиперплазия чаще поражает женщин, постоянно применяющих оральные контрацептивы Аденомы печени имеют практически идентичную картину в В-режиме, и дифференцировка часто требует гистологической оценки.
При использовании цветового и энергетического допплеровских режимов при очаговой узловатой гиперплазии определяется типичная картина кровотока, что позволяет провести дифференциальную диагностику.
Сосудистое сплетение при очаговой узловатьй гиперплазии расходится рааиаиыю от центральной артерии, демонстрируя центрифугальныи кров ток с образованием симптома «спиц колеса».
Очаговая узловая гиперплазия и аденома могут характеризоваться схожей симптоматикой вследствие увеличения за счет роста или кровотечения. При КТ очаговая узловая гиперплазия и аденомы наиболее четко определяются в раннюю артериальную фазу усиления.
В паренхимальную фазу они гипер- или изоэхогенны по отношению к окружающей ткани печени.
Гемангиомы печени
В отличие от очаговой узловатой гиперплазии, гемангиомы кровоснабжаются от периферии к центру. В артериальную фазу наружные области образования усиливаются, тогда как центр остается гипоэхогенным.
Центральная часть становится значительно более эхогенной в последующую воротную фазу, а все образование приобретает гиперэхогенный характер в позднюю венозную фазу.
Эта картина усиления от периферии к центру, также называемая симптомом «диафрагмы радужки», типична для гемангиом печени. Она также определяется при КТ.
Гепатоцеллюлярный рак
Выявление при ультразвуковой допплерографии внутри- и околоопухолевых артериальных допплерипскнх сигналов, обрывов сосудов, сосудистой инвазии, спиральных конфигураций и увеличение количества артериовенозных шунтоэ рассматриваются, как критерии злокачественности.
Гепатоцеллюлярный рак обычно имеет гетерогенную картину усиления сигнала в артериальную фазу после введения контрастного препарата.
Он остается гиперэхогенным в воротную фазу и принимает изоэхогенный характер по отношению к нормальной паренхиме печени в позднюю венозную фазу.
Метастазы в печень
Метастазы в печень могут быть гипо- или гиперваскулярными.
Хотя точное расположение первичной опухоли по сосудистой картине печеночного метастаза определить невозможно, было обнаружено, что для некоторых первичных опухолей характерна определенная степень васкуляризации.
Нейроэндокринные опухоли, такие, как С-клеточный рак щитовидной железы или карциноид, имеют тенденцию к образованию гиперваскулярных метастазов, тогда как метастазы первичных колоректальных опухолей обычно гиповаскулярны.
В артериальную фазу после введения контрастного препарата при стандартной методике сканирования метастазы характеризуются небольшим контрастным усилением в зависимости от степени васкуляризации.
Они обычно остаются гипоэхогенными по отношению к паренхиме печени в позднюю венозную фазу или могут становиться изоэхогенными.
Эта низкая эхогенность в позднюю венозную фазу после введения контрастного препарата является ключевым критерием дифференциальной диагностики метастазов от вышеописанных доброкачественных образований печени Что из этого вытекает? Отличительной характеристикой метастазов является их тенденция к формированию артериовенозных шунтов. Это может объяснить, почему контрастные препараты быстрее выводятся из печеночных метастазов, чем из нормальной паренхимы печени, именно поэтому в позднюю фазу контрастной перфузии картина метастазов относительно гипоэхогенна.
Типичными признаками печеночных метастазов являются неравномерная картина усиления, спиралеобразная или штопорообразная конфигурация сосудов и наличие большого числа артериовенозных шунтов. Вследствие последнего аспекта попадание контрастного вещества в печеночные вены происходит в течение 20 секунд вместо 40 секунд в норме.
Помочь в дифференциальной диагностике между гепатоцеллюлярным раком и метастазами может и клиническая картина: больные гепатоцеллюлярным раком часто страдают от цирроза печени, хронического гепатита и/или имеют повышенный уровень альфа-фетопротеина в крови. Эта комбинация гораздо реже отмечается у больных с печеночными метастазами.
Специальные методики сканирования
При сканировании с низким механическим индексом (МИ ~ 0,1), часто совмещенном с фазовой инверсией, мелкие микропузырьки сразу же разрушаются во время начального прохождения болюса. Это удлиняет контрастное усиление В то же время использование низкого механического индекса снижает чувствительность исследования.
Например, при использовании низкого механического индекса заднее акустическое усиление уже не является эффективным критерием дифференцировки кист от других гипоэхогенных образований.
В некоторых случаях заднее акустическое усиление вновь появляется лишь при подъеме механического индекса до «нормальных» величин от 1,0 до 2,0.
Переменная трансмиссия двух ультразвуковых импульсов в секунду вместо 15 (переменная гармоническая визуализация) позволяет визуализировать даже мельчайшие капилляры, поскольку более длительная межимпульсная задержка ведет к меньшему разрушению микропузырьков. В результате их большая концентрация приводит к капиллярному усилению сигнала, когда отсроченный импульс проходит через ткань.
- При применении методики переменной импульсной трансмиссии при низком механическом индексен даже гиповаскулярные метастазы становятся гиперэхогенными в раннюю артериальную фазу (в течение первых 5-10 секунд от прохождения контрастного вещества), при этом создается видимое различие между ранней артериальной и артериальной фазами контрастного усиления.
- Важное правило дифференциальной диагностики образований печени
- Применение контрастных веществ позволяет использовать следующее диференциально-диагностическое правило: образования с большей продолжительностью усиления сигнала скорее всего являются доброкачественными, тогда как метастазы и гепатоцеллюлярном раке часто гипоэхогенны по сравнению с окружающей паренхимой печени даже в позднюю венозную фазу.
- Воспалительные заболевания кишечника
Несмотря на сложные условия сканирования желудочно-кишечного тракта некоторые патологические состояния можно выявить и оценить с помощью ультразвукового метода.
В-режим позволяет заподозрить воспалительный процесс по наличию экссудата и утолщению стенок кишки Выявление гиперваекуляризации дает возможность предположить хроническое или острое воспалительное заболевание кишечника.
При флюороскопической энтерографии (контрастное исследование тонкой кишки с помощью техники Sellink) определяется сегмент остаточного просвета.
Острый энтерит и лучевой энтерит также характеризуются неспецифической гиперваскуляризацией, что приводит к увеличению скорости кровотока и его объема в верхней брыжеечной артерии. При аппендиците также определяется неспецифическая гиперваскуляризация утолщенной и воспаленной кишечной стенки.
Критическая оценка
Ультразвуковая допплерография является неинвазивной методикой исследования с различными возможностями оценки органов и сосудистых систем брюшной полости. Печень легко доступна ультразвуковому исследованию даже в сложных клинических условиях. Для оценки очаговых и диффузных изменений паренхимы и сосудов печени определены специфические показания.
Ультразвуковая допплерография стала методикой выбора в диагностике и оценке портальной гипертензии, а также в планировании и контроле постановки чрезяремного внутрипеченочного портосистемного шунта. Ультразвуковая допплерография позволяет произвести неинвазивное измерение скорости и объема кровотока, выявить такие осложнения, как стеноз и окклюзия.
Ультразвуковая допплерография используется для послеоперационного контроля трансплантатов печени с целью определения перфузии органа. Однако не существует стандартных критериев, позволяющих поставить диагноз отторжения трансплантата печени.
Характеристика очаговых образований печени основана на степени васкуляризации. Известны некоторые критерии злокачественности, которые помогают более точно диагностировать объемное образование печени. Применение ультразвуковых контрастных препаратов позволяет улучшить отображение васкуляризации и оценить изменения картины перфузии в различные фазы контрастирования.
При исследовании сосудов брюшной полости ультразвуковая допплерография используется для скрининга и оценки аневризм. Для планирования терапевтического и хирургического лечения могут потребоваться дополнительные методы, такие, как КТ, МРТ и ДСА. Ультразвуковая допплерография также является методом скрининга при хронической ишемии кишечника.
Способность ультразвуковой допплерографии выявлять повышенную васкуляризацию при воспалительных заболеваниях, таких, как аппендицит и холецистит, расширила возможности ультразвуковой диагностики.
Опытный специалист УЗИ может определить специализированные нестандартные показания к ультразвуковой допплерографии, используя датчик с высоким пространственным разрешением. Однако существуют и определенные ограничения этого метода. Например, для проведения полного обследования может потребоваться значительное время.
Более того, операторозависимость ультразвуковой допплерографии при обследовании брюшной полости достаточно высока.
Благодаря достижениям в электронной обработке данных результаты исследований будут продолжать улучшаться, становясь более детализированными и легко интерпретируемыми, например, при использовании панорамной техники SieScape и трехмерных реконструкций.
Тканевая гармоническая визуализация является новой методикой, которая используется в диагностически сложных случаях, позволяя улучшить визуализацию при плохих условиях сканирования брюшной полости.
Использование различных контрастных препаратов значительно улучшило возможности ультразвуковой диагностики, особенно у больных с объемными образованиями печени.
Таким образом, ультразвуковая допплерография представляет собой неинвазивную диагностическую методику с высоким потенциалом развития, которая при обследовании брюшной полости обязательно должна применяться значительно шире, чем в настоящее время.
Источник: https://ilive.com.ua/health/uzi-sistemy-vorotnoy-veny_75075i15992.html
Мезоренальное шунтирование
Внепеченочная окклюзия воротной вены и ее притоков — вторая по частоте причина синдрома портальной гипертензии после цирроза печени, следствием которой является 5-10% наблюдений кровотечения из варикозно-расширенных вен верхних отделов желудочно-кишечного тракта [11].
Эта форма портальной гипертензии более характерна для детского возраста, когда она возникает в результате врожденных мальформаций воротной вены, омфалита или посткатетеризационного флебита пупочной вены [5].
У взрослых пациентов портальный тромбоз является следствием цирроза, опухолей гепатопанкреатодуоденальной зоны, миелопролиферативных заболеваний, воспалительных процессов и операций на органах брюшной полости [6].
Декомпрессивное шунтирование является радикальным методом лечения, позволяющим исключить кровотечения из пищеводных и желудочных варикозно-расширенных вен и не приводящим к энцефалопатии и печеночной дисфункции у этой группы больных [7].
В качестве адекватных путей притока для шунтирования при наличии окклюзированной воротной вены могут быть использованы селезеночная или верхняя брыжеечная вена. Тромбоз этих сосудов делает выполнение шунтирующего вмешательства затруднительным, а чаще всего невозможным.
Представляем клиническое наблюдение эффективной портальной декомпрессии у больной с внепеченочной портальной гипертензией и рецидивирующими кровотечениями из варикозно-расширенных вен желудка после прошивания варикозно-расширенных вен пищевода и желудка, спленэктомии и мезокавального шунтирования.
Больная Д., 30 лет, была госпитализирована в одну из центральных районных больниц Новосибирской области с клинической картиной желудочно-кишечного кровотечения. На основании эндоскопического исследования источник кровотечения был определен как «варикозно-расширенные вены пищевода», в связи с чем был установлен зонд Блэкмора и начата стандартная гемостатическая терапия.
Через сутки от момента поступления кровотечение дважды рецидивировало, несмотря на баллонную тампонаду.
По линии санитарной авиации больная была консультирована на месте специалистами Государственной новосибирской областной клинической больницы (ГНОКБ), при повторной эзофагогастроскопии уточнено, что имеется варикозное расширение вен кардиального отдела желудка с переходом на дно III степени, с разрывом одной из варикозно-расширенных вен.
Выполнено эндоскопическое интравазальное склерозирование цианакрилатом и дополнительное эндоскопическое лигирование нескольких варикозно-расширенных вен субкардии лигатором Shooter MBL-U-10 («Cook Medical»), достигнут устойчивый гемостаз. После стабилизации состояния больная через сутки была переведена в ГНОКБ.
Анамнез. В периоде новорожденности больная перенесла омфалит, в 1991 г. (в возрасте 10 лет) — гастротомию, прошивание варикозно-расширенных вен пищевода и желудка, затем в этом же году — спленэктомию, в 1999 г. наложен мезокавальный анастомоз. Все операции выполнялись по поводу рецидивирующих кровотечений из варикозно-расширенных вен пищевода.
Несмотря на выполненное шунтирующее вмешательство, у больной продолжали возникать кровотечения из вен пищевода, в 1999 г. при мезентерикопортографии был диагностирован тромбоз верхней брыжеечной вены и мезокавального анастомоза.
С этого времени ей выполнялась этапная эндоскопическая коррекция варикозного расширения вен пищевода (лигирование и склерозирование), способствовала устранению варикозного расширения вен пищевода.
Объективное обследование при поступлении. Общее состояние средней тяжести. Кожные покровы бледные. Периферических отеков нет. Масса тела 54 кг, рост 166 см. Пульс 92 в 1 мин, АД 110/70 мм рт.ст. Тоны сердца ясные, ритмичные, патологических шумов нет.
Дыхание везикулярное, хрипов нет. На передней брюшной стенке имеются старые гипертрофические послеоперационные рубцы по срединной линии и в левом подреберье.
Живот не вздут, при пальпации мягкий, безболезненный во всех отделах, патологических образований, асцита не определяется, печень не увеличена.
Лабораторные исследования. Анализ крови: Hb 89 г/л, л. 22,1·109/л, эр. 2,99·1012/л, Ht 25,5%, тр. 161·109/л. Все показатели биохимического исследования крови в пределах нормы.
Показатели гемостаза: АЧТВ 30 с, MHO 1,0, фибриноген 3100 мг/л, ХIIа-зависимый фибринолиз 10 мин, агрегация с АДФ 8 с, агрегация с ристомицином 9,5 с, дефектов в системах протеинов С, S, в том числе нарушения резистентности фактора Vа к активированному протеину С, не выявлено.
Эзофагогастродуоденоскопия.
Пищевод свободно проходим, имеются умеренные рубцовые изменения слизистой, варикозное расширение вен нижней трети пищевода до 2 мм, варикозно-расширенные до 5-8 мм вены кардиального отдела желудка с переходом на дно с множественными эрозиями, визуализированы ранее лигированные и склерозированные некротизированные варикозно-расширенные вены без признаков кровотечения, привратник сомкнут, луковица двенадцатиперстной кишки не изменена (рис. 1, а).
Рисунок 1. Гастроскопия (а) до операции. Стрелкой указан некротизированный варикс через сутки после лигирования. Объяснения в тексте. Рисунок 1. Гастроскопия (б) после операции. Заключение: варикозное расширение вен пищевода I степени, варикозное расширение вен желудка III степени, тип GOV2; состояние после эндоскопического склерозирования и лигирования варикозно-расширенных вен желудка (степень варикозного расширения определена по А.Г. Шерцингеру [3], тип — по S. Sarin и A. Kumar [8]).
Мезентерикопортография. Визуализированы кавернозная трансформация воротной вены, фрагмент ствола верхней брыжеечной вены у места ее вероятного слияния с селезеночной веной, расширенный до 6 мм приток верхней брыжеечной вены (рис. 2).
Рисунок 2. Мезентерикопортограмма перед операцией. 1 — портальная кавернома; 2 — фрагмент селезеночной вены: 3 — фрагмент ствола верхней брыжеечной вены за перешейком поджелудочной железы; 4 — левый приток верхней брыжеечной вены.
Таким образом, на основании анамнеза и выполненных обследований был установлен диагноз: внепеченочная окклюзия воротной вены. Синдром портальной гипертензии. Варикозное расширение вен пищевода I степени.
Варикозное расширение вен желудка III степени, тип GOV2, осложненное кровотечением. Прошивание варикозно-расширенных вен пищевода и желудка (1991 г.). Спленэктомия (1991 г.). Мезокавальное шунтирование (1999 г.
), тромбоз мезокавального анастомоза.
В данной ситуации с учетом наличия осложненного варикозного расширения вен желудка, паллиативного характера его эндоскопической коррекции, ангиографической картины было решено выполнить портосистемное шунтирование.
Перенесенное мезокавальное шунтирование и, следовательно, рубцовые изменения в области инфраренального сегмента нижней полой вены предполагали серьезные технические трудности при повторном мезокавальном шунтировании.
Принимая во внимание последнее, а также локализацию проходимого левого притока верхней брыжеечной вены (единственного «шунтабельного» сосуда портального бассейна по данным мезентерикопортографии), решили использовать в качестве пути оттока интактную левую почечную вену.
Больная оперирована в объеме Н-образного аутовенозного мезоренального шунтирования трансплантатом из левой внутренней яремной вены. В условиях эпидуральной анестезии с ИВЛ выполнена бисубкостальная лапаротомия. Разделены множественные сращения в верхнем отделе брюшной полости.
Асцита нет, печень обычного цвета, не увеличена в размерах, поверхность гладкая, край острый, вены желудка, большого сальника, брыжейки тонкой кишки расширены. Других патологических изменений не выявлено. Из окружающих тканей выделен и мобилизован на протяжении 4 см левый приток верхней брыжеечной вены диаметром 6 мм под перешейком поджелудочной железы.
Основной ствол вены постфлебитически изменен и втянут в рубец в проекции инфраренального отдела нижней полой вены. Мобилизован нижнегоризонтальный отдел двенадцатиперстной кишки. Выделена и мобилизована на протяжении 4 см антеаортально расположенная левая почечная вена.
Линейным разрезом по медиальному краю кивательной мышцы слева выделена левая внутренняя яремная вена диаметром 6 мм, фрагмент длиной 4 см забран для использования в качестве трансплантата, центральная и дистальная культи яремной вены ушиты.
Выполнено боковое отжатие левой почечной вены зажимом Сатинского, приток верхней брыжеечной вены выключен из кровотока клампами Де Бейки. Последовательно сформированы анастомозы аутовенозного трансплантата в изогемодинамической позиции с левой почечной и верхней брыжеечной венами нитью пролен 6/0 growth factor (рис. 3).
Рисунок 3. Вид сформированного Н-образного мезоренального шунта. 1 — левый приток верхней брыжеечной вены; 2 — левая почечная вена; 3 — восходящий отдел двенадцатиперстной кишки. Сняты зажимы с вен. Портосистемный градиент до пуска кровотока составил 20 мм рт.ст., после пуска кровотока снизился до 7 мм рт.ст. Взят биопсийный материал из края III сегмента печени, при гистологическом исследовании данных, свидетельствующих о циррозе и активном гепатите, нет.
Больная экстубирована через 3 ч при нормальных показателях газообмена и гемодинамики. Послеоперационный период протекал без осложнений, пациентка выписана в удовлетворительном состоянии через 10 сут после операции без признаков постшунтовой энцефалопатии.
Перед выпиской выполнена контрольная эзофагогастродуоденоскопия, при которой отмечена полная редукция варикозно-расширенных вен пищевода и желудка (см. рис. 1, б).
Через месяц после выписки выполнена МСКТ-ангиография, при которой визуализирован проходимый мезоренальный шунт (рис. 4).
Рисунок 4. Мультиспиральная компьютерная томограмма после операции. 1 — левый приток верхней брыжеечной вены; 2 — левая почечная вена.
На момент написания статьи срок наблюдения составляет 8 мес, состояние больной удовлетворительное, кровотечения не рецидивировали, эндоскопических признаков варикозного расширения вен пищевода и желудка нет.
Возможности коррекции внепеченочной портальной гипертензии включают медикаментозную терапию, эндоскопические методы устранения варикозного расширения вен пищевода и желудка и хирургические вмешательства: разобщающие процедуры, различные варианты портосистемного шунтирования и мезопортальное (Rex) шунтирование [9].
Последнее признано на сегодняшний день предпочтительным вариантом реконструкции, позволяющим осуществить портальную реперфузию печени [10], но вместе с тем не всегда выполнимым, особенно при посткатетеризационном флебите пупочной вены [4]. По данным А.Ю. Разумовского, у детей с внепеченочной окклюзией воротной вены выполнение Rex-шунтирования возможно в 30-35% наблюдений [2].
Спленэктомия у больных с синдромом портальной гипертензии была довольно популярной в прошлом веке, что объяснялось положительным влиянием ее на портальное давление и клеточный состав периферической крови.
В настоящее время доказано, что удаление селезенки не является адекватным вмешательством при синдроме портальной гипертензии, так как не способствует снижению портосистемного градиента, при котором не развиваются кровотечения, увеличивает риск тромбоза шунтов в послеоперационном периоде и в большинстве наблюдений приводит к тромбозу селезеночной вены — гемодинамически и анатомически удобного притока для шунтирования [12]. Шунтирующие процедуры позволяют решить проблему гиперспленизма и наиболее эффективно снижают вероятность кровотечений из варикозно-расширенных вен [2]. К сожалению, следует признать, что до сих пор больным с предпеченочной формой портальной гипертензии нередко производятся паллиативные разобщающие вмешательства и спленэктомии, усложняющие выполнение радикальных реконструкций и, следовательно, ухудшающих отдаленные результаты лечения больных с предпеченочной портальной гипертензией. Такой анамнез в сочетании с неэффективным портосистемным шунтированием в большинстве наблюдений переводит изначально прогностически благоприятный вариант блока портального кровотока в разряд «нешунтабельной» портальной гипертензии. Мезоренальное шунтирование является нестандартным и редким вариантом портальной декомпрессии, который можно использовать в подобной ситуации. При анализе литературы мы встретили лишь единичное описание данной операции, выполненной ребенку [1], публикаций подобных клинических наблюдений у взрослых больных мы не нашли.
Источник: https://www.mediasphera.ru/issues/khirurgiya-zhurnal-im-n-i-pirogova/2012/6/030023-12072012613

 желудок.
желудок.